Konference: 2011 XVIII. Jihočeské onkologické dny
Kategorie: Gastrointestinální nádory
Téma: Nádory žaludku
Číslo abstraktu: 19
Autoři: MUDr. Adam Peštál; Prof. MUDr. Ivan Čapov, CSc.; doc. MUDr. Václav Jedlička, Ph.D.; MUDr. Jan Žák, Ph.D.; MUDr. Jan Doležel, Ph.D.; MUDr. Martin Veselý, Ph.D.; MUDr. Zdeněk Chovanec
Metoda:
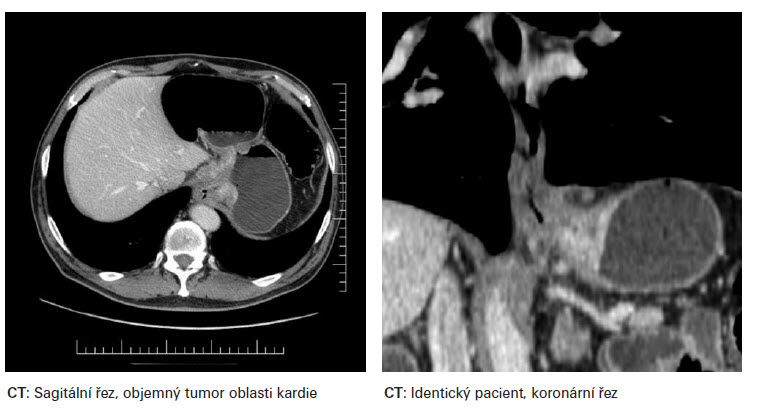
Strategie léčby adenokarcinomu oblasti EGJ je dána stadiem onemocnění. Toto je určeno nadále exaktním stanovením TNM parametrů. Diagnostika parametru T se opírá o CT,GF a též o endosonografický nález. Diagnostika N stadia, využívá dále i PET a FNB. Možná je i laparoskopická diagnostika, výjimečně VATS (videotorakoskopie). K chirurgické léčbě je určeno primárně stadium I. a II. U stadia II. je indikovaná pooperační adjuvantní chemoterapie u high risk T2N0 - v případě G3, lymfovaskulární invaze, neurovaskulární invaze a mladého věku pacientů. Dále v případě T3N0, T1-2 N1. Možná je i perioperační chemoterapie ECF (3 cykly před operací, 3 cykly po operaci). Stadium III. je indikované k chirurgické léčbě v případě dobré odpovědi na neoadjuantní onkoterapii. Neoadjuvantní léčba zvyšuje počet radikálních operací. Onkologická léčba po chirurgickém resekčním výkonu je dále též korigovaná typem resekce - R0, R1 a definitivním pTpNpM. Typ resekčního výkonu můžeme stanovit pomocí Siewertova doporučení, klasifikace adenokarcinomu oblasti EGJ.
Diskuze:
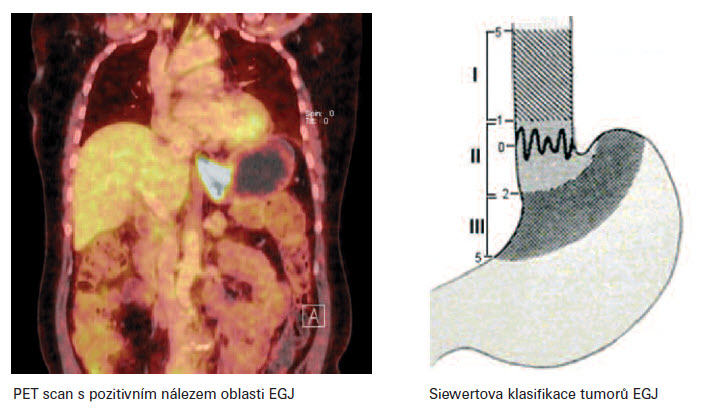
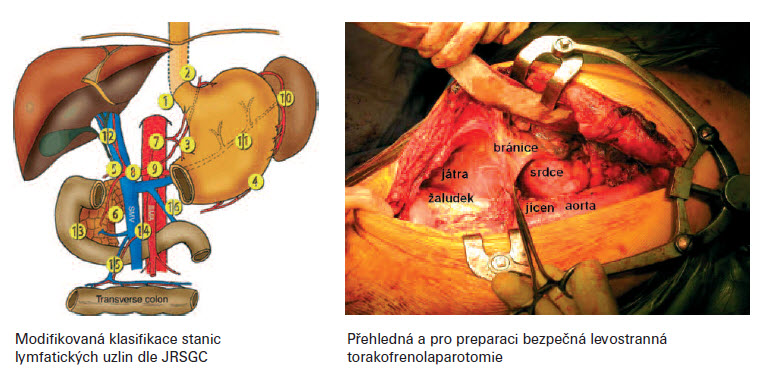
Siewertova klasifikace adenokarcinomu lokalizovaného v oblasti kardie (Siewet et. al 1987 Mnichov) dělí tumory do tří typů. Typ I. - centrum tumoru leží 1-5cm orálně od EGJ. Typ II. - centrum tumoru infiltruje EGJ, tumor je lokalizovaný od 1 cm orálně až 2 cm aborálně od junkce. Typ III. - centrum tumoru je lokalizovano 2-5 cm pod EGJ. Dle Siewertovy klasifikace, je pak stanoven typ chirurgického resekčního výkonu. Pro typ I. se jedná o subtotální esofagektomii s proximální resekcí žaludku s lymfadenektomií paraezofageální a horního břišní kompartmentu. K obnovení kontinuity zažívacího traktu je možno využít gastropastiku zbylé části žaludku (velká křivina, antrum) či interpozitum kličkou jejuna dle Rouxe či koloplastiku. Pro typ II. a III. je indikována totální gastrektomie s distální resekcí jícnu a lymfadenektomií dolního mediastina s D2 břišní lymfadenektomií. Obnovení zažívacího traktu je konstruováno zpravidla jejunoplastikou. Součástí chirurgických resekčních výkonů je i omentektomie. V literatuře je možno se setkat i s „maximálním" resekčním výkonem typu totální gastrektomie se subtotální ezofagektomií s koloplastikou. Výkon je ale zpravidla zatížen vysokou morbididou doprovázenou i vyšší mortalitou. Invaze tumoru do bránice, jater - T4 v případě N0-1, za předpokladu případné resekability R0, není po neoadjuvantní léčbě s dobou odpovědí kontraindikací k chirurgické léčbě. V případě totální gastrektomie provádíme lymfadenektomii typu D2, lymfadenektomii D1 nepovažujeme za dostatečnou. Evropskými autory popisovaná vyšší morbidita i mortalita spojena s lymfadenektomií typu D2 je dána předně technickou peroperační komplikací, při které dochází ke krvácení a vynuceně ke splenektomii či resekci pankreatu, které nejsou běžnou součástí chirurgické léčby. Zásadní je lymfadenektomie v bezprostředním okolí tumoru, kompletní resekce malého omenta a lymfadnektomie oblasti a. gastrica sinistra a trunkus celiakus. S paraezofageální lymfadenektomií a lymfadenektomií oblasti bifurkace trachei nebývají zpravidla technické potíže. Spádové lymfatické uzliny žaludku dělíme dle modifikované klasifikace dle JRSGC (Japanese Research Society for Gastric Cancer) do tří kompartementů. Lymfatické uzliny stanice 1.-6. tvoří I., 7.-11. II. a 12.-16. III. kompartment. Dle některých autorů tvoří LU skupiny 15. a 16. kompartement IV. Lymfadenektomie typu D1 spočívá v odstranění uzlin a přilehlé tukové tkáně kompartmentu I., D 2 I. a II. Dle TNM klasifikace tvoří metastázy v LU III. kompartementu marker M1. Skupiny lymfatických uzlin dle stanic: 1. parakardiální při malé křivině, 2. parakardiální při velké křivině, 3. uzliny podél malého zakřivení žaludku, 4. podél velkého zakřivení, 5. podél suprapylorické, 6. infrapylorické, 7. uzliny podél a. gastrica sinistra, 8. podél a. hepatica communis, 9. v oblasti truncus coeliacus, 10. v oblasti hilu sleziny, 11. podél av. lienalis, 12. oblast ligamentum hepato-duodenale, 13. retropankreaticky v oblasti hlavy slinivky břišní, 14. podél av. mesenterica superior, 15. podél av. colica media, 16. podél abdominální aorty.
Výsledky:
Na I. chirurgické klinice LF MU a FN u sv. Anny v Brně je strategie léčby stanovena multioborovou komisí. Stran chirurgické léčby se řídíme Siewertovou klasifikací. Při typu I. preferujeme subtotální esofagektomii a anastomózou cervikální vlevo s gastroplastikou.V případě, že je tumor rozsáhlý a není možno stanovit zcela exaktně klasifikaci před operací, je možno nález korigovat peroperačně. Výjimečně, není-li ani pak zcela zřejmé, že se jedná o typ I. či II. indikujeme totální gastrektomii s vysokou resekcí jícnu a jejunoplastokou sec. Roux. Nutné je vždy též peroperační vyšetření resekční linie jícnu, makroskopicky nelze hodnotit pro častou submukózní invazi tumoru. Nutritivní jejunostomie nebývá konstruována, konstruujeme ji dodatečně, až v případě komplikací ve smyslu fistuly v anastomóze. Tuto komplikaci jsme měli v průběhu posledních 5 let jen ve dvou případech a to v oblasti krční anastomózy. Oba pacienti jsou dnes bez potíží. V případě, že nejsou klinické známky komplikací, jsou pacienti zatěžováni stravou od šestého dne. V případě jakýchkoli pochybností, např. pooperační febrilie, pneumonie,... je pasáž zažívacím traktem indikována. Pacienti mohou přijímat vodu bez bublin po malých porcích ihned první pooperační den. Chirurgickým přístupem je nejčastěji levostranná torakofrenolaparotomie. Nepozorovali jsme pooperační komplikace v souvislosti s frenotomií. Pacienti leží na pravém boku, operační pole je velmi přehledné a pro preparaci bezpečné. Selektivní ventilace, respektive kolaps levé plíce je vyžadován vždy jen na dobu nezbytně nutnou ve spolupráci s anesteziologem. Je tedy možno během rozličných fází operace ventilovat na obě plicní křídla a kolaps plíce vyžadovat jen dle potřeby. Stran typu anastomózy, tedy gastroesofageální či jejunoesofageální, je možno tuto konstruovat end-to-end, ručně či častěji pomocí cirkulárního stapleru, nebo side-to-end, respektive side-to-side. Druhý typ anastomóz je námi preferovaný. Používáme modifikovanou Orringerovu semimechanickou anastomózu, kdy zadní obvod je konstruován pomocí lineárního endostapleru 45 mm/4,8 mm. Přední obvod šit ručně ve dvou vrstvách. Anastomóza je konstruována na provlečené dekompresní sondě, kterou ponecháváme do 6. pooperačního dne. Interjejunoanastomóza je šita zpravidla koncem ke straně ručně, ve dvou vrstvách. V případě komplikací s netěsnosti anastomózy doporučujeme aktivní léčbu. Drenáž mediastina, pohrudniční dutiny, literárně jsou velmi dobré výsledky s překrytím defektu v oblasti netěsnosti hrudní anastomózy samorezorbovatelným stentem. Máme vlastní (jedinou) zdárnou zkušenost s aplikací explantabilního stentu na defekt krční anastomózy.
Závěr:
Diagnostika nádorového onemocnění EGJ je multioborová, terapie zpravidla multimodalitní. Vzájemná vstřícná spolupráce jednotlivých specialistů je zásadní. Přesné stanovení stadia choroby a správně zvolená strategie léčby by měla být záležitostí odborných komisí. Péče o pacienty by měla být koncentrována do pracovišť schopných komplexně zajistit v plném rozsahu jak diagnostiku, tak léčbu, včetně možných souvisejících komplikací. Chirurgické pracoviště by mělo plně zvládat problematiku hrudní chirurgie. S ohledem na stoupající incidenci refluxní choroby, Barretova jícnu, patrně se stravovacími návyky, živostním stylem, tabakismem,... lze předpokládat i v budoucnu nadále potřebu kvalitní, moderní, účinné terapie adenokarcinomu ezofagogastrické junkce.
Literatura:
-
NCCN Practice Guidelines in Oncology - v 1. a 2. 2010.
-
ESMO Clinical Recommedations, Annals of Oncolocy (Supplement 4) 2009.
-
Zásady cytostatické léčby maligních onkologických onemocnění 11. vydání ČOS.
-
Siewert JR., Holsher A H., Becker K., Gossner W., Cardia cancer: attempt at a therapeutically relevant classification, Chirurgie 1987,58, 25-32.
-
Siewert J. R., Stein H. J., Bottcher K., Lymphadenektomie bei tumoren des oberen Gastrointestinaltrakts, Chirurg 1996, 67: 877-888.
-
Feith M., Stein H. J., Siewert J. R. Adenocarcinoma of the esophagogastric junction: surgical therapy based on 1602 consecutive resected patients, Surg Oncol Clin N Am 2006; 15:751764
Datum přednesení příspěvku: 14. 10. 2011
