Konference: 2012 3. pražské mezioborové onkologické kolokvium Prague ONCO
Kategorie: Zhoubné nádory prsu
Téma: Review
Číslo abstraktu: 005
Autoři: prof. MUDr. Petra Tesařová, CSc.
V rámci medicínského pokroku se farmakologický výzkum soustředí především na vývoj cílené léčby onkologických onemocnění, která slibuje účinnější likvidaci nádoru s menším množstvím nežádoucích účinků. Na základě výsledků klinických studií byla do praxe zavedena řada nových léků, které vykazují vysokou efektivitu. Přesto je jejich prospěšnost limitovaná nástupem získané rezistence. Rezistenci na cílenou léčbu je třeba včas rozpoznat. Intenzivně probíhá také výzkum, jak ji překonat. (1)
Nejčastější zhoubný nádor žen – karcinom prsu, je velmi heterogenní onemocnění. Cílenou léčbu je možné využít jen tehdy, pokud to dovolí přítomnost specifických terčů na povrchu nebo uvnitř nádorových buněk, jako je HER2 neu receptor, nebo receptor pro estrogen (ER) či progesteron (PR).
HER2 neu receptor je overexprimován zhruba u 10-15 % pacientek s karcinomem prsu a jeho přítomnost je spojena s horší prognózou nemoci. V současné době máme k dispozici dva léky zacílené na HER2 neu receptor, monoklonální protilátku trastuzumab, která prokázala statisticky významnou účinnost nejen v paliativní, ale i v adjuvantní léčbě. Její podání je standardem adjuvantní léčby HER2+ nemocných po celý rok a zároveň standardem první linie léčby metastatického onemocnění. Ve druhé linii léčby metastatického onemocnění je indikován tyrozinkinázový inhibitor lapatinib, pronikající i přes hematoencefalickou bariéru. V praxi denně řešíme problém, jak neukončit léčbu trastuzumabem, ze kterého může nemocná ještě profitovat, příliš brzy a naopak, abychom nepodávali lék v situaci naprosté rezistence, kdy pacientku ohrožujeme progresí nemoci a především vznikem mozkových metastáz.(2)
Předpokládané mechanismy rezistence na trastuzumab:
1) Porucha vazby trastuzumabu na receptor:
a) Zkrácený receptor – metaloproteinázy způsobí uvolnění extracelulární domény HER2 neu. Intracelulární doména pak není schopná vázat trastuzumab.
b) Maskování receptoru pomocí glykoproteinu mucin 4 (MUC4) nebo adhezní molekulou CD44. Trastuzumab není schopen rozpoznat vazebné místo.
2) Zvýšená aktivace HER2 metabolické cesty:
a) Ztráta PTEN – mutací způsobená ztráta tumor supresorového genu PTEN (fosfatáza a tenzin homolog) přítomná zhruba u 50 % pacientek s karcinomem prsu zvyšuje aktivaci PI3K/ATK (fosfatidylinozitol 3-kináza), takže ji trastuzumab není schopen účinně blokovat.
b) Konstitutivní aktivace PI3K/ATK, způsobená mutací podjednotky p85α, opět ruší účinnost blokády trastuzumabu.
c) PDK1 overexprese je další možnou příčinou rezistence.
d) Modulace inhibitoru cyklin dependentní kinázy p27 dalšími léky může rušit efekt trastuzumabu.
3) Alternativní signální cesty:
a) zvýšená signalizace pomocí dalších členů HER rodiny (HER1, HER3);
b) zvýšení signálů jiných receptorů – IGFR1, VEGFR, met, ER, cyklin E, TNFα, EPO, rac 1 atp.).
Obrázek 1: Mechanismy rezistence k trastuzumabu
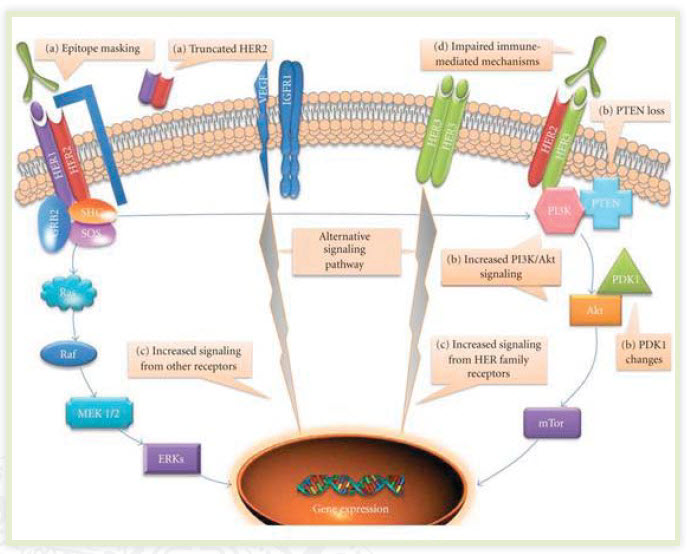
4) Porucha imunitní odpovědi – hlavním mechanismem cytotoxického účinku trastuzumabu je na protilátkách závislá buněčná imunita (ADCC), pokud je její mechanismus narušen, není funkční ani terapie trastuzumabem.(3)
Léčebné možnosti překonání rezistence k trastuzumabu:
- změna chemoterapie přidané k trastuzumabu;
- lapatinib;
- lapatinib + trastuzumab;
- TDM1;
- trastuzumab + pertuzumab;
- trastuzumab + everolimus;
- neratinib;
- tanespimycin + trastuzumab
Rezistence k hormonální léčbě
Hormonální léčba představuje pro pacientky s karcinomem prsu nejenom další léčebnou možnost, rozšiřující spektrum terapeutických nástrojů, ale také záruku relativně dobré kvality života nemocné. Je tedy velmi závažné, pokud se nádor stane k hormonální terapii rezistentním. Asi 50 % nemocných s pozitivitou hormonálních receptorů je k hormonální léčbě primárně rezistentních, téměř všechny nemocné dlouhodobě léčené pro generalizovaný karcinom prsu ztratí postupně citlivost k hormonální léčbě. (4)
Velmi slibnou cestou překonání obou typů rezistence – primární i získané, se zdá být kombinace hormonální léčby s mTOR inhibitorem. Jeho aktivace totiž ruší blokádu hormonálního receptoru antihormonální léčbou. mTOR hraje významnou roli v proliferaci, buněčném cyklu, angiogenezi, apoptóze, homeostáze a má i řadu metabolických funkcí, ovlivňuje například i funkci lymfocytů.
Obrázek 2: Mechanismus možného ovlivnění rezistence k hormonální léčbě blokádou mTOR
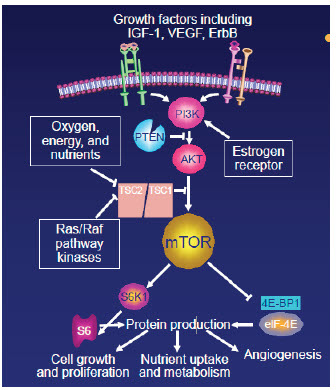
H. Rugo, San Antonio, 2012, PRIME
Efektivitu tohoto teoretického předpokladu ověřila jak studie fáze II TamRad, porovnávající léčbu tamoxifenem a tamoxifenem s everolimem u generalizovaných nemocných s hormonálně dependentním karcinomem, ale i studie Bolero 2, kombinující exemestan s everolimem oproti samotnému exemestanu u pomenopauzálních ER+ nemocných s metastatickým karcinomem prsu. Po 12 měsících došlo k prodloužení doby do progrese v kombinovaném rameni o 4,2 měsíce.
U HER2 pozitivních nádorů se současnou expresí hormonálních receptorů je hormonální léčba rušená stimulací HER2 receptoru, proto může být účinná jedině při současné blokádě HER2 neu receptoru.(5) Další možností léčby pro hormonálně rezistentní pacientky zůstává chemoterapie.
Závěr
Rezistence k cílené léčbě bude pravděpodobně ještě dlouho problém, který budeme řešit v našich ambulancích pravidelně. Nicméně teprve pochopení pravděpodobných mechanismů jejího vzniku nám pomůže do budoucna, doufám, stále častěji volit takovou léčbu, která prodlouží možnost co nejdelšího přínosu z cílené léčby generalizovaných pacientek s karcinomem prsu.(6)
doc. MUDr. Petra Tesařová, CSc. Onkologická klinika 1. LF UK a VFN, Praha e-mail: petra.tesarova@lf1.cuni.czLiteratura
- Higgins MJ, Baselga J. Targeted therapies for breast cancer. J Clin Invest 2011;121(10):3797-803.
- Brügmann A, Sorensen BS. Identifying responders to trastuzumab therapy in breast cancer. Future Oncol 2011;7(6):767-73.
- Arribas J, Baselga J, Pedersen K, Parra-Palau JL. p95HER2 and breast cancer. Cancer Res 2011;71(5):1515-9.
- Bodmer A, Castiglione-Gertsch M. Role of hormonal manipulations in patients with hormone-sensitive metastatic breast cancer. Eur J Cancer 2011;47 Suppl 3:S28-37.
- Khokhar NZ, Altman JK, Platanias LC. Emerging roles for mammalian target of rapamycin inhibitors in the treatment of solid tumors and hematological malignancies.Curr Opin Oncol 2011;23(6):578-86.
- Burstein HJ. Novel agents and future directions for refractory breast cancer. Semin Oncol 2011;38 Suppl 2:S17-24.
Datum přednesení příspěvku: 24. 9. 2012
